2026年2月,深圳大学医学部公共卫生学院刘甲野课题组在免疫学领域国际期刊《Frontiers in Immunology》(中科院大类二区期刊)发表题为“Persistent CD8⁺ T cell-driven immune dysregulation despite normalized CD4⁺ T cell recovery in ART-treated people with HIV”的研究论文。医学部硕士研究生胡艺耀与葛凌云为论文共同第一作者,深圳大学刘甲野与解放军总医院第五医学中心张超副教授为共同通讯作者,深圳大学为第一作者单位和主要通讯作者单位。
 1-1
1-1
虽随着ART的广泛应用,HIV感染者(PWH)的CD4⁺ T细胞水平通常可以恢复至正常范围,但仍有相当一部分患者存在CD4/CD8比值持续倒置的现象,这种“免疫不协调恢复”与心血管疾病、肿瘤等非艾滋病相关并发症风险升高密切相关。然而,其背后的细胞与分子机制尚不清楚。
本研究基于5,416例接受长期ART治疗的PWH队列,采用基于轨迹建模的方法,首次从动态角度识别出不同的CD8⁺ T细胞演变模式,并将人群划分为免疫调节恢复组(IMR)和慢性稳定激活组(CSA)。研究发现,尽管两组患者均实现CD4⁺ T细胞恢复,但CSA组表现出持续升高的CD8⁺ T细胞水平及CD4/CD8比值倒置,提示存在长期免疫失衡状态。
进一步通过多组学联合分析(CyTOF免疫表型分析、bulk RNA测序及血浆炎症因子检测),研究系统揭示了该免疫异常的关键特征:CSA组患者表现为效应性和衰老型CD8⁺ T细胞显著扩增、调节性T细胞减少,并伴随IP-10、MCP-1、CD163等炎症因子水平升高,提示持续性系统炎症状态。此外,转录组分析显示该人群中免疫炎症通路、趋化因子信号通路及抗原呈递相关通路显著激活,进一步支持CD8⁺ T细胞驱动的免疫失调机制。
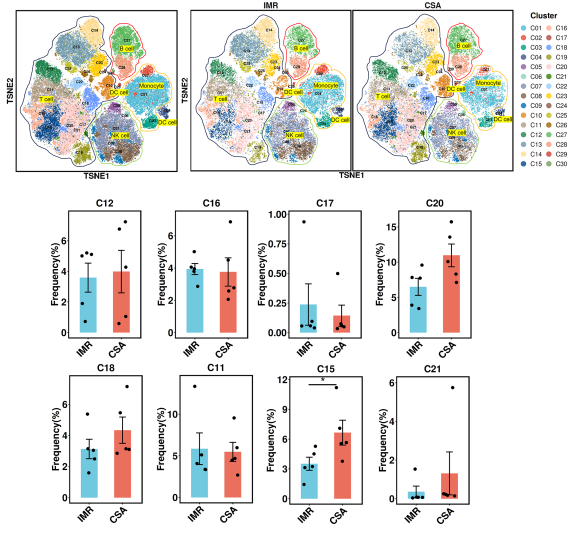
研究表明,即使在病毒学抑制和CD4⁺ T细胞恢复的情况下,CD8⁺ T细胞持续激活仍代表一种独立的免疫异常状态,可能成为预测非艾滋病相关并发症的重要免疫学标志物。该研究从群体动态、细胞表型及分子机制多个层面,系统阐明了HIV感染者免疫重建不完全的关键路径,为未来靶向CD8⁺ T细胞调控的干预策略提供了重要依据。
该研究得到国家自然科学基金面上项目、广东省及深圳市相关科研项目资助。
原文链接:https://www.frontiersin.org/journals/immunology/articles/10.3389/fimmu.2026.1735779/full




用户登录
还没有账号?
立即注册