程永现/罗奇合作OL|灵芝驱动的新发现:罕见硫/砜基骨架分子从内生真菌中发现
程永现/罗奇合作OL|灵芝驱动的新发现:罕见硫/砜基骨架分子从内生真菌中发现

图1灵芝内生真菌及其罕见含硫/砜基骨架分子
内生真菌作为真菌生物多样性的重要组成部分,广泛寄生于植物、动物以及大型真菌等宿主中。在与宿主协同进化的过程中,内生真菌形成了独特的生物合成机制,能够产生结构复杂的次级代谢产物。这些产物不仅具有生态功能,如参与与宿主的相互作用、发挥竞争抑制作用,还具备一定的药用潜力,包括抗菌、抗癌等功效。
最新研究显示,目前已从内生真菌中鉴定出超过143种含硫天然产物,主要包括非核糖体肽、聚酮、萜类及其杂合分子。值得一提的是,在经美国食品药品监督管理局(FDA)批准的药物中,含硫原子的药物占比达20%,例如抗生素类的青霉素G和头孢菌素C、抗癌药物曲背替定以及降脂药瑞舒伐他汀等(图2)。
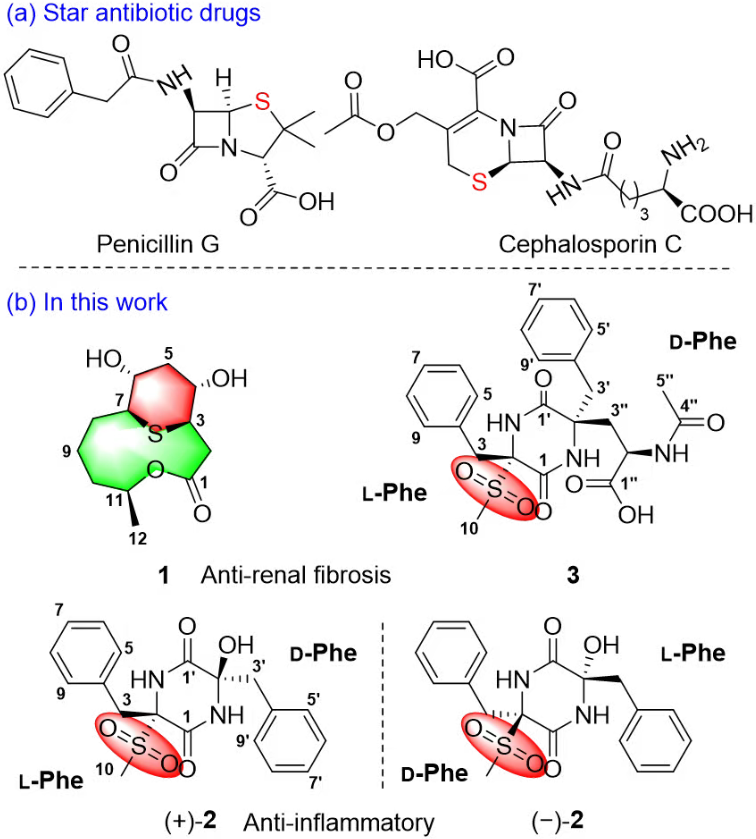
图2含硫的明星小分子药物及化合物1-3的化学结构
鉴于含硫真菌代谢物具有独特的结构特征和显著的生物活性,其受到了天然产物和合成化学科学界的广泛关注。含硫的天然产物,尤其是那些含有砜部分的天然产物,属于自然界中结构独特且较为罕见的次级代谢物。截至目前,仅有3例相关报道来自内生真菌,6例来自海洋微生物,这充分体现了此类含硫天然产物的稀缺性。
近期,南方医科大学中医药学院罗奇教授与深圳大学药学院程永现教授团队合作,从名贵中药灵芝内生真菌Ascomycota sp. GLQ01和Trichoderma harzianum GLQ03中发现了4个前所未有的含硫/砜基骨架小分子。其中,Ascomycotols A (1)具有一种新颖的聚酮小分子,具有罕见的4-oxa-12-thiabicyclo[7.3.1]十三烷骨架。另外,Ascomycotols B (2)和Ascomycotols C (3)具有不同寻常的砜基结构特征,实属罕见(图2)。最终,通过光谱数据、量子化学计算和X射线衍射确定它们的立体绝对构型(图3)。

图3化合物1的X射线衍射图
生物合成途径推测方面(图4)。首先,化合物1的生物合成路径:(1)前体生成阶段:化合物1的生物合成始于聚酮合酶(PKS)与硫酯酶(TE)结构域的协同作用,通过1分子乙酰辅酶A与5分子丙二酰辅酶A的缩合反应生成关键前体A。该过程涉及聚酮链的逐步延伸与硫酯酶介导的链释放,形成线性聚酮中间体。(2)大环化反应:中间体B通过羧酸与羟基的缩合反应形成十二元大环结构(如chloriolide)。此步骤依赖于酶促催化,可能涉及分子内亲核攻击或酸催化机制,最终完成大环骨架的构建。(3)硫桥形成与氧化修饰:生物合成的最终阶段通过两次连续的S-亲核加成反应形成含硫桥的六元环结构。阳离子中间体D经氧化酶催化生成终产物1,其分子中引入两个羟基,推测与黄素依赖性氧化酶或细胞色素P450酶系相关。
其次,化合物2与3的生物合成路径:(1)二酮哌嗪(DKP)核心的合成:化合物2和3的结构分析表明,其骨架由两个苯丙氨酸(Phe)残基通过肽键缩合形成二酮哌嗪(DKP)核心。该过程由非核糖体肽合成酶(NRPS)介导,通常包含L-Phe和D-Phe的非典型组合。值得注意的是,NRPS模块中D-Phe的引入可能通过转氨酶或消旋酶实现,导致终产物(±)-2和3的立体化学多样性。(2)立体化学多样性来源:D-Phe的非典型掺入可能源于NRPS系统中特定腺苷甲硫氨酸(SAM)依赖性甲基转移酶或消旋酶的调控。这种立体选择性机制在天然产物生物合成中较为罕见,可能与基因簇中辅助酶的协同作用相关。(3)磺酰基团的罕见性与生物学意义:磺酰基(-SO₂-)在天然产物中直接存在的案例较少,其生物合成途径尚未完全阐明。现有研究显示,磺酰基可能通过硫代酶或硫氧还蛋白系统引入,但相关酶的催化机制仍需进一步验证。磺酰基团的引入可能增强分子的亲脂性或参与金属离子螯合,但其在天然产物中的功能仍需结合生物活性研究进行验证。例如,磺酰基可能通过调节分子构象或增强氢键作用影响靶点结合。

图4化合物1-3的生物合成途径
在化合物1-3抗炎初筛中,化合物1与(+)-2均显著抑制IL-6、IL-1β及MCP-1 mRNA表达,证实潜在抗炎活性(图5)。因(+)-2存量仅0.5 mg的限制性瓶颈,后续优先推进化合物1的衰老相关肾纤维化活性研究。

图4化合物1-3的生物合成途径
在化合物1-3抗炎初筛中,化合物1与(+)-2均显著抑制IL-6、IL-1β及MCP-1 mRNA表达,证实潜在抗炎活性(图5)。因(+)-2存量仅0.5 mg的限制性瓶颈,后续优先推进化合物1的衰老相关肾纤维化活性研究。

图5 化合物1和(+)-2抑制LPS诱导RAW 264.7细胞中炎症介质的mRNA表达。
通过KEGG通路富集分析,我们发现细胞衰老通路在化合物1作用下呈现显著富集(p<0.05)。这一发现为后续机制研究提供了明确的分子生物学框架,提示该化合物可能通过调控衰老相关信号通路发挥治疗作用。研究结果显示,在D -半乳糖(D-gal)诱导的NRK-52e细胞中,1以剂量依赖的方式显著抑制纤连蛋白和I型胶原(collagen I)(图6A),以及EMT关键标志物α-SMA(α-SMA)的表达。另外,考虑到细胞p16和p21的上调与年龄相关疾病有关,我们进一步研究了化合物1对p16和p21蛋白表达的影响。结果显示,化合物1使得p16和p21均表达下调,证实了化合物1在年龄相关肾纤维化中的功效(图6B)。

用户登录
还没有账号?
立即注册