陈玮琳教授团队在 Cell Death & Differentiation发表USP43/RNF2轴调控抗病毒固有免疫研究成果
2025年3月,深圳大学医学部基础医学院陈玮琳教授团队在《Cell Death & Differentiation》(影响因子13.7,TOP期刊,中科院一区)发表题为“The USP43/RNF2 axis negatively regulates antiviral innate immunity by promoting TBK1 ubiquitination and degradation”的研究论文,阐明了去泛素化酶USP43能够去泛素化稳定E3泛素连接酶RNF2,进而促进TBK1泛素化降解,负向调控细胞及机体抗病毒固有免疫反应。医学部助理教授赵西宝和狄乾乾为本研究共同第一作者,陈玮琳特聘教授为本文唯一通讯作者。

固有免疫系统是抵抗和清除病毒入侵的重要防线,研究固有免疫应答的机制,探寻固有免疫应答的调控分子,是近年来的前沿研究热点。蛋白翻译后受到多种形式修饰,这些修饰调控着蛋白生物学功能,影响众多细胞生命活动。蛋白泛素化及去泛素化修饰在抗病毒固有免疫中起到重要作用,但是其分子机制还未完全阐明,尤其E3泛素连接酶自身被泛素化修饰调控及其在抗病毒固有免疫中的作用,尚不清楚。
本研究表明USP43在体内外能够显著负调病毒诱导的I型干扰素及干扰素刺激下游基因的表达,提示USP43负向调控抗病毒固有免疫。利用定量蛋白质组学质谱分析,发现USP43通过促进TBK1泛素化降解负向调控I型干扰素产生。USP43是一种去泛素化酶,而本研究发现USP43能够促进TBK1泛素化降解,提示中间涉及其它E3泛素连接酶。结合多组学质谱分析(Co-IP混合物质谱分析和泛素化修饰定量蛋白质组学质谱分析)和机制研究,明确了USP43通过去泛素化稳定E3泛素连接酶RNF2,从而促进TBK1泛素化降解,负向调控抗病毒固有免疫应答。本研究阐明了USP43/RNF2轴在调控细胞及机体抗病毒固有免疫中的作用,揭示了泛素连接酶RNF2自身泛素化修饰的调控过程,为病毒感染性疾病的防治提供新的见解和潜在治疗靶点。
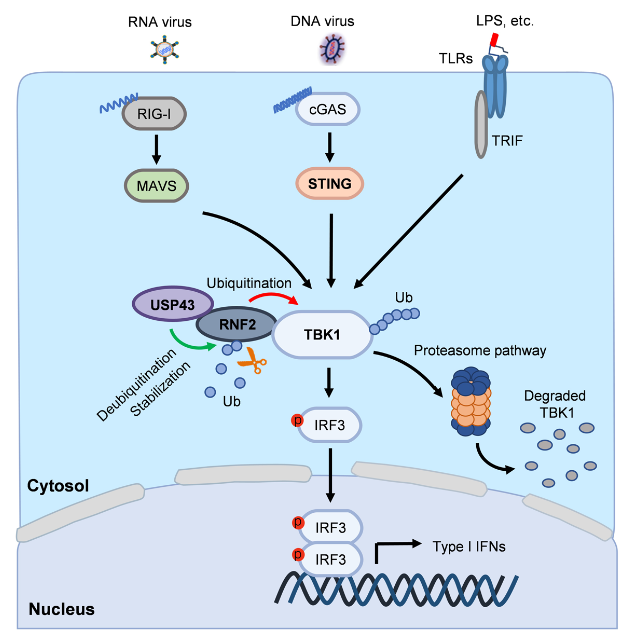
本研究得到国家自然科学基金、广东省自然科学基金和深圳市科创委等项目的资助。
原文链接:https://doi.org/10.1038/s41418-025-01491-x


用户登录
还没有账号?
立即注册