医学部许兴智教授团队在Nucleic Acids Research发文揭示有丝分裂核心激酶PLK1活性的新调控机制
近日,医学部许兴智教授团队在《Nucleic Acids Research》(影响因子16.971)发表了题为“PARP1 and CHK1 coordinate PLK1 enzymatic activity during the DNA damage response to promote homologous recombination-mediated repair”的原创研究成果。报道揭示了DNA损伤应答过程中有丝分裂核心激酶PLK1(Polo-like kinase 1)活性调控的崭新机制。医学部基础医学院助理教授彭斌为论文第一作者,许兴智教授为通讯作者。
PLK1是真核生物中高度保守的丝氨酸/苏氨酸蛋白激酶,参与了中心体的成熟、有丝分裂期的启动、纺锤体的形成、染色体的排列、染色体的分离和胞质分裂及DNA复制等诸多重要的生命活动。PLK1在增殖旺盛的细胞中表达,而成体组织不表达或表达水平很低。研究表明PLK1在多种人类肿瘤中都高度表达,包括乳腺癌,非小细胞肺癌和结直肠癌等,而且PLK1的表达与不良的预后密切相关。因此,PLK1也是药物设计及抗肿瘤的明星靶点。
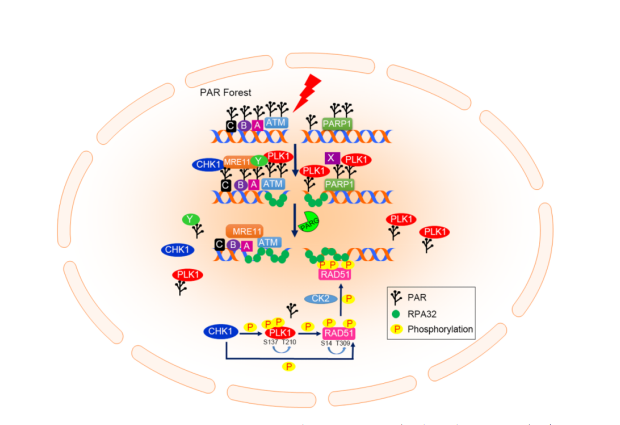
相对于PLK1在有丝分裂中的功能,在DNA损伤应答过程中PLK1活性变化存在争议,其调控机制更是不得而知。David Stern实验室发现DNA损伤发生后PLK1激酶活性会被抑制(Cell Cycle, 2005);Fumiko Esashi实验室报道了PLK1活性在DNA双链断裂后20-40分钟会被短暂激活(Molecular Cell, 2012),并直接对同源重组(HR)修复的重组酶RAD51的S14进行磷酸化,从而促进了RAD51在染色质上的加载和HR介导的DNA双链断裂修复。我们发现在DNA损伤应答过程中PLK1的活性在时空和空间上受到精确的调控:(1)DNA双链断裂发生后,PLK1瞬时被募集到DNA损伤位点,该募集依赖于多聚ADP核糖(PAR)聚合酶PARP1的活性及其产物PAR;(2)PLK1与PAR的结合直接抑制其激酶活性;(3)PLK1从DNA损伤位点处解离到核质中(依赖于PAR水解酶PARG);(4)在核质中,结合了PAR的PLK1被CHK1在S137位点磷酸化进而促进了其T210位点的磷酸化,从而活化PLK1;(5)活化的PLK1对核质中RAD51 S14位点进行磷酸化,引发CHK1对RAD51的T309位点磷酸化修饰;(6)该PARP1/CHK1-PLK1-RAD51 信号轴最终促进HR)介导的DNA修复并确保染色体稳定性和细胞放射敏感性。我们的研究诠释了在DNA损伤应答过程中PLK1活性的动态变化及其调控机制,揭示了PLK1的S137位点磷酸化修饰是T210位点的磷酸化修饰和PLK1激活的先决条件,为PARG和 CHK1 抑制剂的联合化疗提供了生物学基础。
《Nucleic Acids Research》为国际知名期刊(中科院JCR1区,TOP期刊)。该课题组的研究依托深圳大学广东省基因组稳定性与疾病防治重点实验室、卡尔森国际肿瘤中心和马歇尔生物医学工程实验室,获得了国家基金委、广东省重点实验室和深圳市科创委的资助。










用户登录
还没有账号?
立即注册