医学部常港团队在《Nature Communications》发表研究论文揭示哺乳动物雄性生殖细胞命运转变的调控机制
“子又有子,子又有孙;子子孙孙无穷匮也”。繁衍生息是一个物种能够长久存在的前提。在高等生物中,生殖细胞承载了将遗传物质在亲代与子代间进行传递的作用,这也构成了生命繁衍的物质基础。生殖细胞的发育调控机制是发育生物学领域的重大科学问题之一,也是我们了解人类不孕不育疾病发生的基础。深圳大学医学部常港团队主要聚焦于探索哺乳动物生殖细胞发育的基础和应用研究,研究团队于2018年在Cell旗下顶级期刊《Cell Stem Cell》(影响因子24.633)发表题为Single-Cell RNA Sequencing Analysis Reveals Sequential Cell Fate Transition during Human Spermatogenesis研究论文(常港博士为本文共同第一作者,在国际上首次揭示了人类成年男性精子发生过程中的基因表达调控网络与细胞命运转变过程,为男性不育的临床诊断提供了新的思路。2021年,研究团队在Cell旗下《Stem Cell Reports》(影响因子7.765)杂志发表题为The Chromatin Accessibility Landscape Reveals Distinct Transcriptional Regulation in the Generation of Human Primordial Germ Cell-Like Cells from Pluripotent Stem Cells研究论文(常港博士为本文共同通讯作者,揭示了SOX15-ETV5调控轴通过抑制体细胞谱系的分化,进而调控人类原始生殖细胞的体外形成和命运维持,为利用多能干细胞体外诱导获得功能性的单倍体生殖细胞奠定了基础。
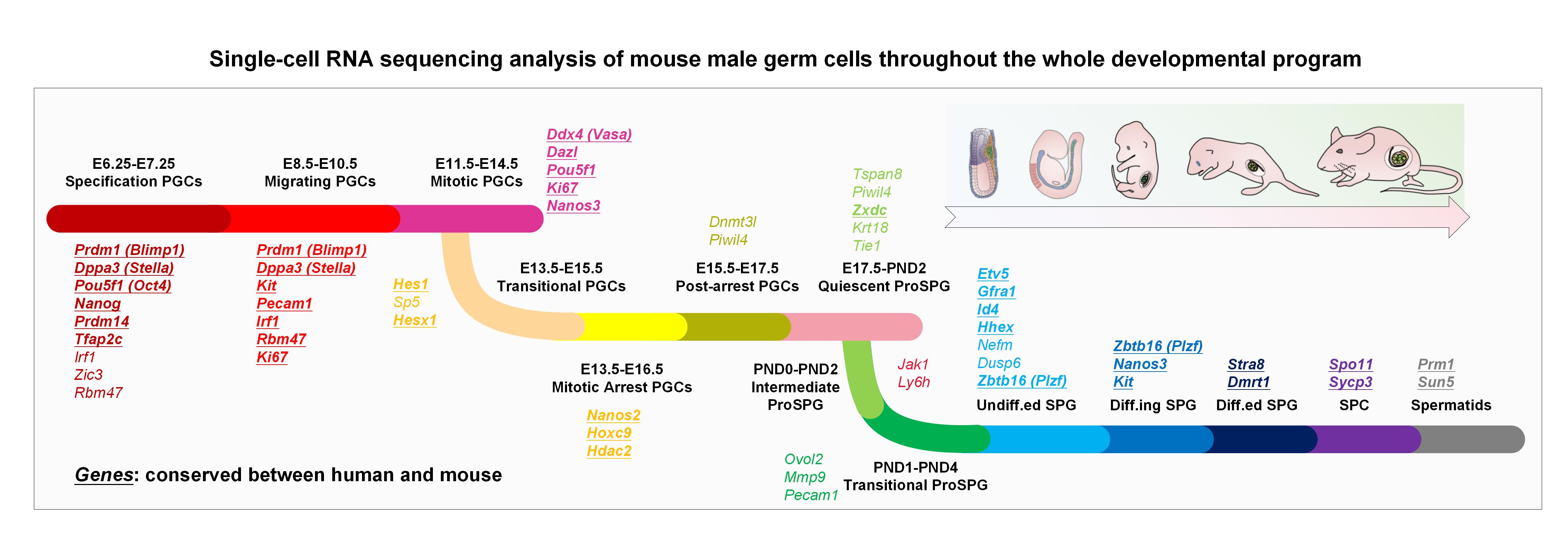
2021年11月25日,医学部常港团队与国内的研究组合作在《Nature Communications》(影响因子14.919)杂志发表题为Cell-fate transition and determination analysis of mouse male germ cells throughout development的研究论文。该研究系统地阐明了哺乳动物雄性生殖细胞的命运转变过程和调控机制,发现转变期原始生殖细胞(Transitional PGC)是一类重要的过渡态细胞亚群,揭示了Notch信号通路在有丝分裂阻滞过程中的关键调控功能,并利用Helq敲除小鼠模型证明了胚胎期生殖细胞的身份转变对于雄性生育力的维持至关重要,最后通过整合数据鉴定出人-鼠生殖细胞高度保守的调控因子。这一工作首次报道了迄今为止最为全面、精度最高的哺乳动物雄性生殖细胞发育图谱,建立的高质量数据集为解析哺乳动物生殖细胞命运决定的调控机制提供了精准坐标,也为生殖细胞的体外诱导分化和男性不育治病机制的探索提供了理论参考。
该课题依托深圳大学医学部生物化学与分子生物学系研究平台完成。常港博士为本文的共同通讯作者和并列第一作者,深圳大学为本文的通讯单位。此项工作得到国家自然科学基金面上项目(31970787、32170869)、广东省自然科学基金面上项目(2019A1515010446)和深圳市基础研究重点项目(JCYJ20210324120212033)等的资助。










用户登录
还没有账号?
立即注册