医学部林静教授团队在Advanced Science发表异二聚体前药酶组装体用于释放抗肿瘤制剂的研究成果
近日,深圳大学医学部生物医学工程学院林静特聘教授团队在国际知名学术期刊《Advanced Science》(影响因子14.3,中科院一区,TOP期刊)上发表了题为“Self-Boosting Programmable Release of Multiple Therapeutic Agents by Activatable Heterodimeric Prodrug-Enzyme Assembly for Antitumor Therapy”的研究论文。医学部博士后江珊珊和Bhaskar Gurram为共同第一作者,林静教授为通讯作者,深圳大学为第一完成单位。该团队所在的生物医学工程学科属于广东省优势重点学科。

内源性刺激反应性前药因其病变特异性和降低全身毒性而被广泛用于抗肿瘤治疗。然而,肿瘤微环境中活性氧(ROS)含量有限,难以实现预期的药物释放。葡萄糖氧化酶(GOx)通过产生大量H2O2提高ROS激活前药效率,但消耗O2会导致肿瘤缺氧,影响O2依赖药物疗效。Ⅰ型光敏剂对O2依赖低,与GOx联用可促进药物释放,实现饥饿与其他治疗协同抗癌。
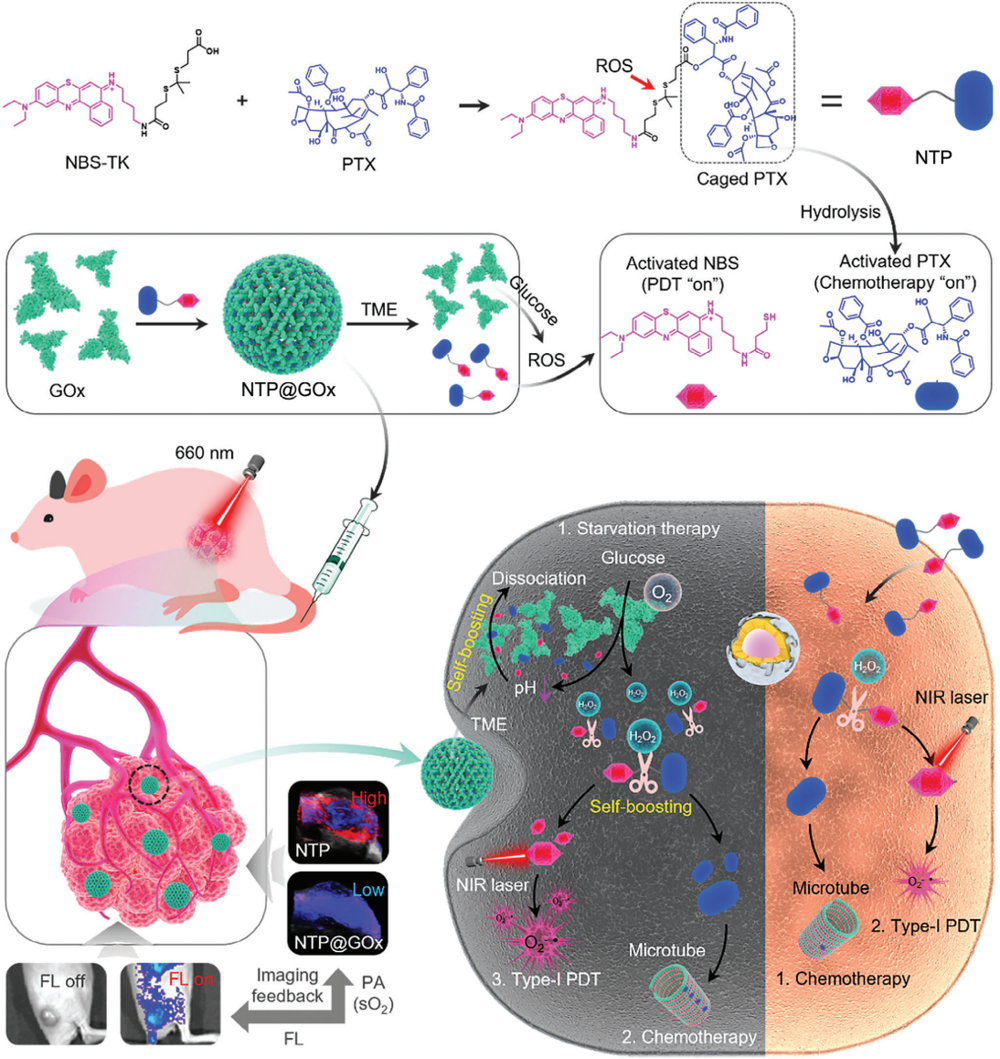
本研究开发了一种由ROS激活的异二聚体前药负载酶组装体,用于自增强程序化释放多种治疗剂,实现高效地抗肿瘤治疗。异二聚体前药NBS-TK-PTX(即NTP)由Ⅰ型PSs (NBS)、紫杉醇(PTX)和ROS响应型硫酮(TK)连接键组成。NTP与GOx有较强的亲和力,通过疏水相互作用形成NTP@GOx组装体。值得注意的是,NTP@GOx中GOx的酶活性被NTP抑制。自增强程序化释放治疗剂过程通过以下步骤实现:首先,NTP@GOx在酸性TME中部分解离,释放出一小部分NTP和GOx,并恢复GOx的酶活性;其次,GOx触发的pH降低进一步促进NTP@GOx的解离,加速了NTP和GOx的大量释放;最后,前药NTP的TK连接键被GOx催化产生的H2O2切断,加速NBS和PTX的释放。在荧光和光声双模态成像引导下,NTP@GOx组装体展现出GOx介导的饥饿治疗、PTX诱导的化疗和基于NBS的Ⅰ型光动力治疗的协同抗肿瘤疗效。
本研究得到了国家重点研发计划、国家自然科学基金、深圳市科技计划基础研究、中国博士后科学基金等项目的支持。
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/advs.202409960










用户登录
还没有账号?
立即注册